 关注我们
关注我们


近日,永乐高ylg官网病理科蓝辉耀教授团队在《Advanced Science》期刊发表了题为“SARS-CoV-2 N protein induces acute kidney injury via Smad3-dependent G1 cell cycle arrest mechanism”的文章(DOI:10.1002/advs.202103248)。该文章通过超声微泡技术,首次证实SARS-CoV-2 N蛋白在急性肾损伤中的致病性。SARS-CoV-2 N蛋白可与TGF-β1下游信号分子Smad3发生相互作用,导致G1细胞周期阻滞,造成肾小管上皮细胞坏死,从而直接造成急性肾损伤。
急性肾损伤(Acute kidney injury, AKI)在病情危重的新冠肺炎患者中较常见,其特征包括血清肌酐水平上升和肾小管坏死,根据已发表的数据显示,在住院的重症新冠肺炎患者中,AKI的发病率超过40%,而且死亡率明显升高。同时有研究表明AKI是继急性呼吸衰竭之后,新冠肺炎危重患者中第二常见的并发症,研究新冠病毒感染引起急性肾损伤的具体机制至关重要。
研究团队利用超声微泡技术,在小鼠肾脏特异表达新冠病毒N蛋白,发现N蛋白可以直接诱导AKI,表现为肾小管坏死、促进血清肌酐水平升高,此现象在缺血-再灌注模型中更加明显,这点与已发表的临床数据非常吻合。

超声微泡介导的肾脏特异性SARS-CoV-2 N蛋白过表达可诱导及加重AKI
进一步研究发现SARS-CoV-2 N蛋白通过与Smad3信号分子相互作用,激活细胞死亡途径、诱发AKI。通过对Smad3基因敲除鼠以及使用特异性Smad3抑制剂的动物研究,他们发现敲除Smad3基因以及抑制Smad3磷酸化可以显著降低新冠病毒N蛋白诱导的细胞死亡和AKI,提出Smad3可作为治疗新冠病毒感染导致AKI的新药物靶标。

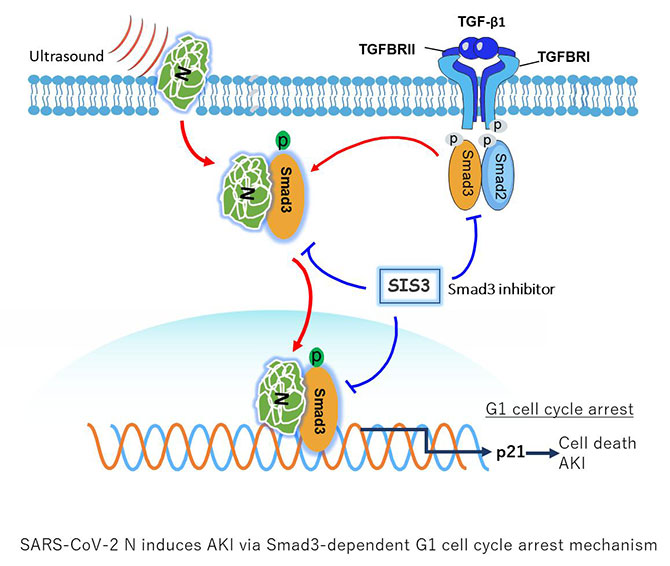
SARS-CoV-2 N蛋白诱导AKI依赖于Smad3

Smad3抑制剂(SIS3)可抑制SARS-CoV-2 N蛋白诱导AKI
永乐高ylg官网蓝辉耀教授、余学清教授、暨南大学吴建国教授为论文的通讯作者和共同通讯作者,永乐高ylg官网引进人才王文标博士和南方医科大学陈俊哲博士为第一作者和共同第一作者,该项研究得到香港研究资助局(14101121)、粤港澳慢性肾病免疫与遗传研究联合实验室计划(2019B121205005)、吕志和创新医学研究所(心血管发展、研究和教育计划)、香江学者计划(XJ2019052) 以及国家自然科学基金(81902053)的支持。
蓝辉耀教授是永乐高ylg官网病理科2019年柔性引进人才,目前担任香港中文大学医学院副院长,李嘉诚健康医学研究所副所长,炎症性疾病研究室主任,香港科学资深主席,亚太免疫学第二届学术委员会副主任,亚太基础免疫学会副主任,世界中医联合会免疫专业委员会副会长,粤港澳大湾区卫生与健康专家顾问,主要研究领域是TGF-β/Smad 信号在免疫炎症性疾病(包括高血压、糖尿病相关性心血管和肾脏疾病、肿瘤微环境)的作用。主持美国NIH, 澳大利亚NH&MRC, 香港RGC,HMRF,ITF等研究基金70多项。发表SCI 365篇,被引用>3.5萬余次,h-指數為104。
文_王文标,图_陈俊哲