 关注我们
关注我们


肾移植是治疗终末期肾病的首选途径,但T细胞介导的排斥反应仍是造成移植肾失功的重要诱因。目前,临床上防治排斥反应主要通过术后静脉应用抗T细胞的免疫诱导药物,但这种全身性的用药会造成严重的感染。因此,寻求一种可靶向作用于移植肾的新免疫诱导方案,将对肾移植术后急性排斥的防治具有重大意义。
孙启全教授团队自主研发了一种同时具备锚定细胞表面和保留PD-L1生物学功能的新型重组蛋白map-PD-L1(图1)。研究证实,map-PD-L1锚定结合内皮细胞的能力与蛋白的孵育浓度和孵育时间呈正比,重点是map-PD-L1的锚定能力受低温环境的影响较小(图2)。同时,map-PD-L1通过结合PD-1,激活PD-1/PD-L1通路,进而抑制T细胞活化和促进T细胞凋亡(图3)。因此,团队利用大鼠肾移植模型,证实离体阶段map-PD-L1可锚定修饰供肾,使得供肾血管内皮细胞表面高表达PD-L1,减少移植肾局部T细胞的浸润,同时可促进Treg细胞(一种免疫调节细胞)在供肾局部的分化,从而改善移植术后排斥反应介导的移植肾损伤,改善移植肾功能,延长移植肾及受体的存活(图4)。
该研究充分利用供体器官离体阶段的独特特点,对供体器官进行特异性锚定修饰,为器官安装好“防弹衣”,从而有效避免全身应用带来的风险,有望为器官移植术后提供一种靶向器官的免疫诱导新方案,实现移植受者的精准治疗,具有重要的临床转化前景及社会意义。
该研究完全由孙启全教授团队独立完成,并于2022年4月5日在中科院1区工程技术领域权威杂志Bioengineering & Translational Medicine(IF:10.711)在线发表(Ex Vivo Anchored PD-L1 Functionally Prevent In Vivo Renal Allograft Rejection;doi.org/10.1002/btm2.10316)。孙启全教授为论文的唯一通讯作者,永乐高ylg官网肾移植科罗子寰医师、廖涛医师和张燕楠助理研究员为共同第一作者,该项研究得到国家自然科学基金(81970650, 82100797, 81770753, 81800663, 81800661, 81800662)和国家重点研发项目(2018YFA0108804))等基金支持。
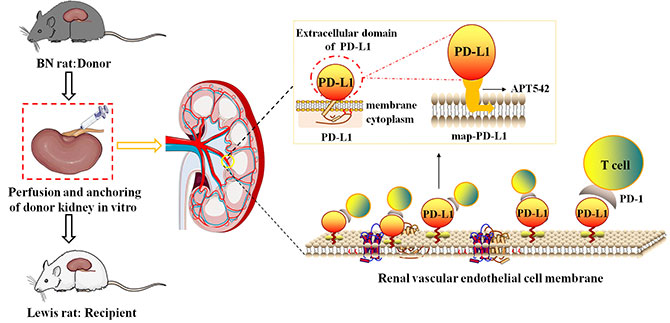
图1. map-PD-L1体外锚定修饰离体供肾的示意图。
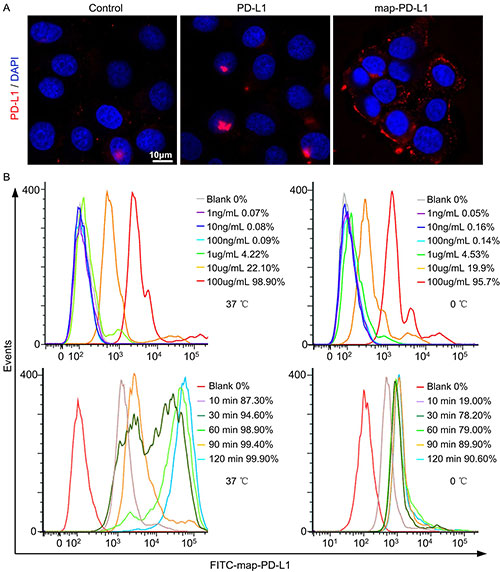
图2. map-PD-L1锚定内皮细胞表面与孵育浓度、孵育时间和温度的关系。
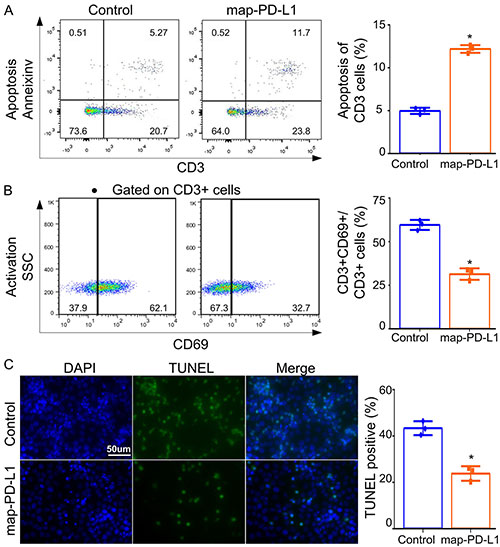
图3. map-PD-L1促进T细胞凋亡并抑制T细胞活化,减少混合培养下受T细胞的杀伤引起的内皮细胞凋亡。
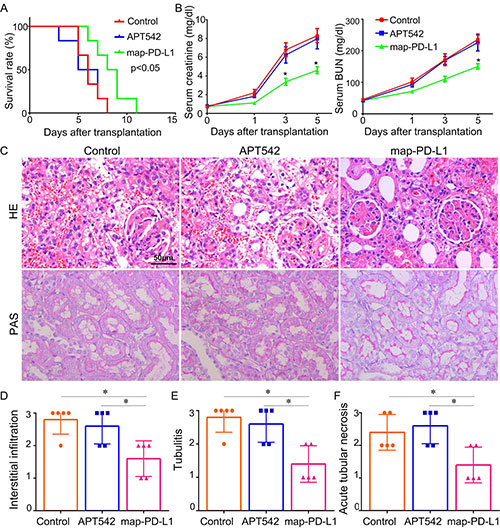
图4. map-PD-L1减轻排斥反应介导的损伤,改善移植肾功能,延长受体存活。
文:罗子寰,图:廖涛